Пептидная регуляция старения
Статья является кратким изложением монографии В. Х. Хавинсона. Пептидная регуляция старения. Издание 3-е, испр. – СПб.: Наука. 2015. 50 с. Введение На протяжении многих лет феномен старения рассматривался преимущественно в рамках этических и социальных проблем. Однако за последнее столетие стало очевидно, что этот процесс имеет определенное эволюционное значение и требует исследования как специальный физиологический механизм организма. Фундаментальные открытия Значительный прорыв в понимании механизмов старения был достигнут благодаря работам выдающихся ученых. И.И. Мечников еще в конце XIX века разработал фагоцитарную теорию иммунитета и доказал связь между повышением клеточного иммунитета и увеличением продолжительности жизни. В последующие десятилетия были сделаны важнейшие открытия в области структуры ДНК, генетической регуляции синтеза белка и расшифровки генетического кода. Эти открытия заложили основу для современных исследований механизмов старения. Механизмы старения При старении происходит постепенная инволюция тканей и нарушение функций организма. Ключевым фактором является изменение структуры клеточного ядра. Хроматин существует в двух формах: эухроматин и гетерохроматин. При старении объем гетерохроматина увеличивается с 63 % до 80 %, что приводит к снижению синтеза белка. Первым при старении страдает иммунитет. Экстракты тимуса и содержащиеся в них короткие пептиды были первыми веществами, использованными для коррекции возрастных иммунодефицитов. Позже выяснилось, что короткие пептиды — универсальные регуляторы: они способны передавать биологическую информацию, воздействовать на гены, стимулировать синтез белка. После открытия протеасомной деградации стало понятно, как организм получает пул коротких регуляторных пептидов. Они могут влиять на экспрессию генов, включая и выключая их, восстанавливая нарушенные функции. Особенно активны такие пептиды в ядерных белках, например, в транскрипционных факторах. С возрастом увеличивается доля гетерохроматина — "молчаливых" участков ДНК, и уменьшается активный эухроматин, что приводит к снижению синтеза белков. Пептиды способны восстанавливать баланс, "разблокируя" нужные участки ДНК. Разработка метода исследования
Тканеспецифичность и регенерация
Генетический уровень действия Пептиды способны:
Основные выводы Исследования показали, что короткие пептиды обладают рядом уникальных свойств:
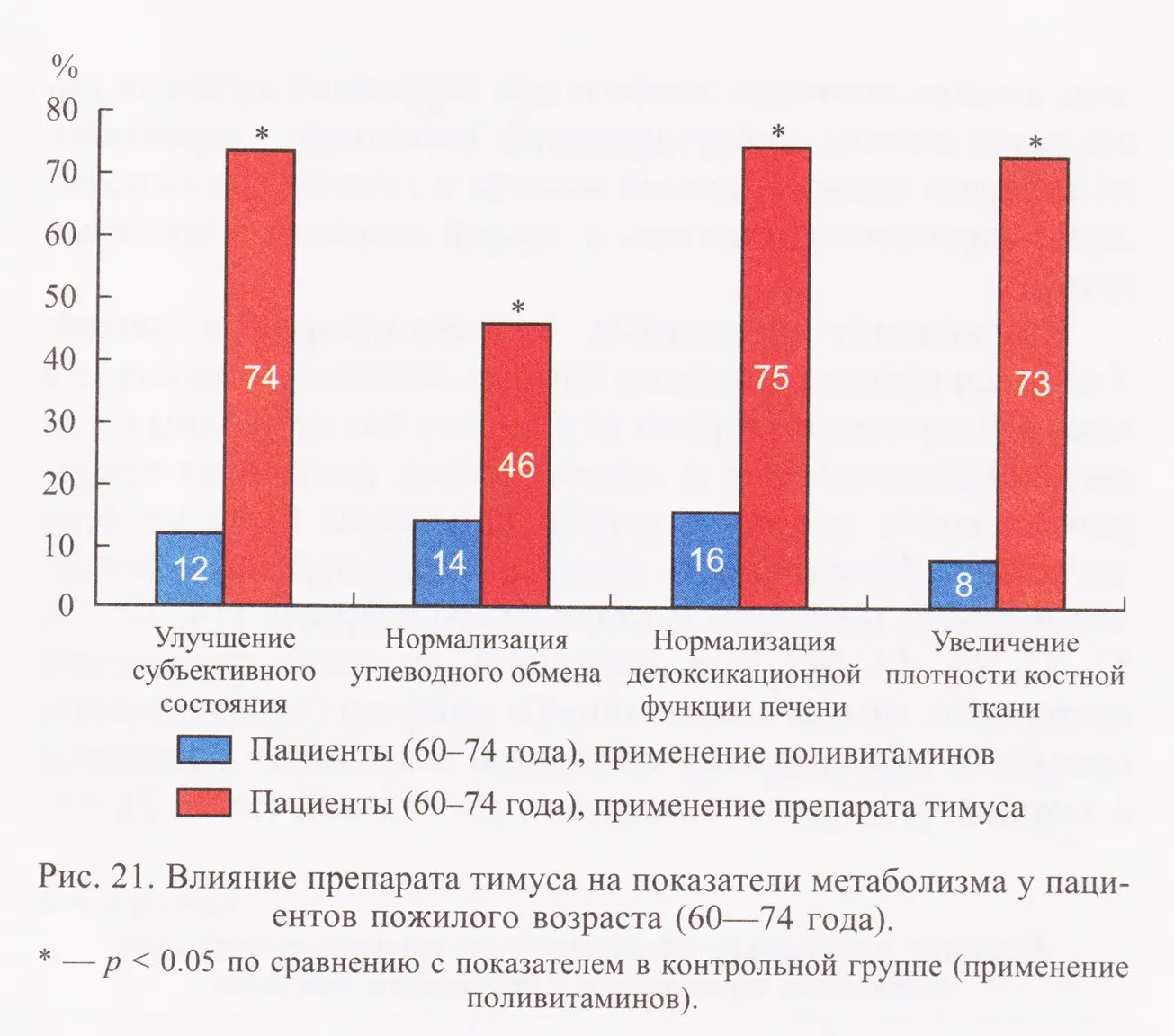
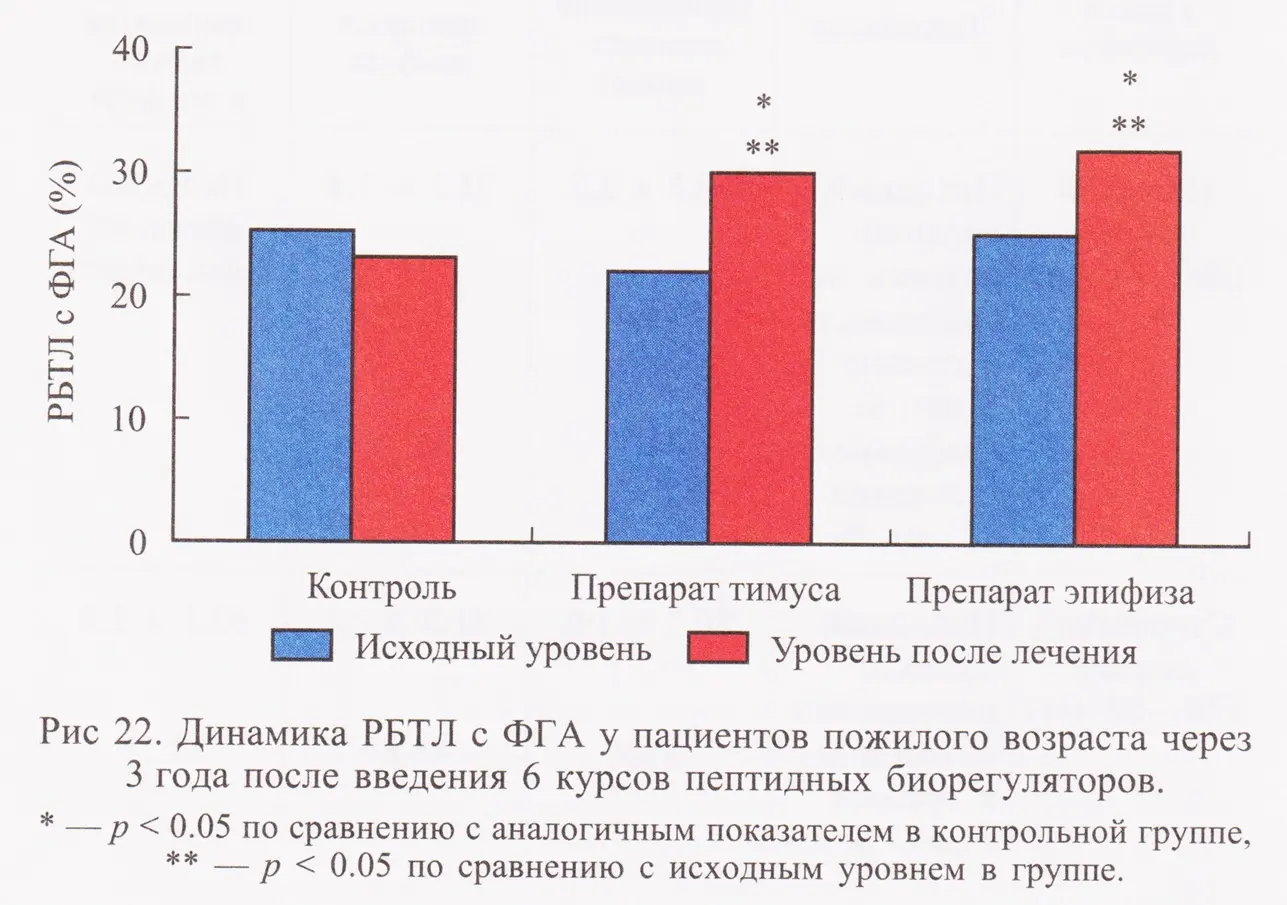
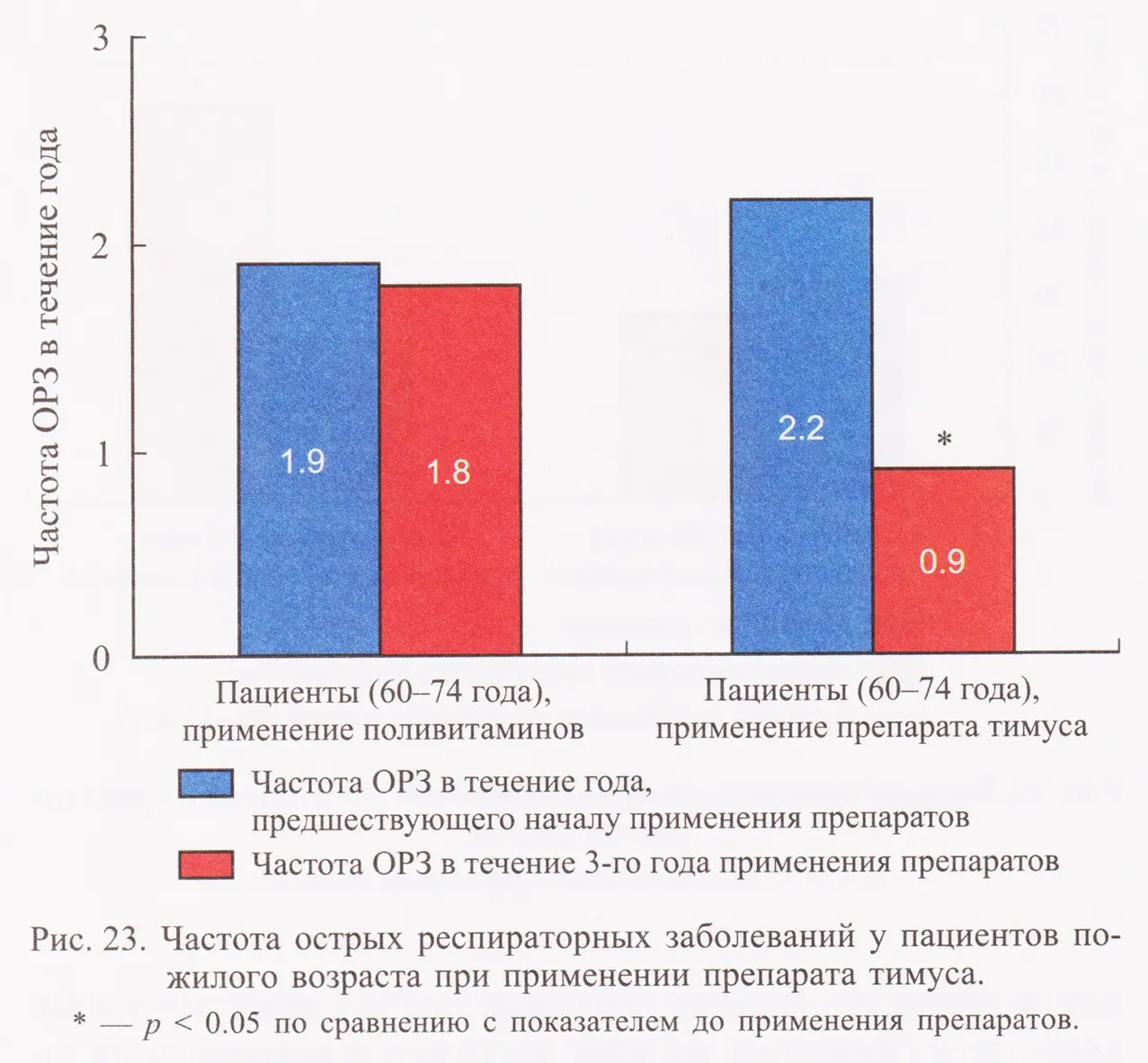
Клинические исследования Многолетние исследования на людях показали высокую эффективность пептидной терапии. Ежегодное применение пептидных препаратов привело к снижению смертности пациентов, улучшению функций иммунной и эндокринной систем, к повышению плотности костной ткани (рис. 21, 22) и снижению частоты респираторных заболеваний в 2 раза (рис. 23).
Яркой клинической эффективностью обладает пептидный препарат, выделенный из сетчатки глаза животных. Этот уникальный препарат впервые был применен у больных при различных дегенеративных заболеваниях сетчатки, в том числе при диабетической ретинопатии, инволюционной дистрофии, пигментной дегенерации сетчатки и при другой патологии. Особенно важной явилась способность препарата восстанавливать электрическую активность сетчатки, что, как правило, коррелировало с улучшением функции зрения. Клинические испытания подтвердили безопасность и эффективность пептидной терапии. Препараты получили более 15 миллионов человек, эффективность лечения составила 75-85 %. Примеры терапевтической активности пептидов:
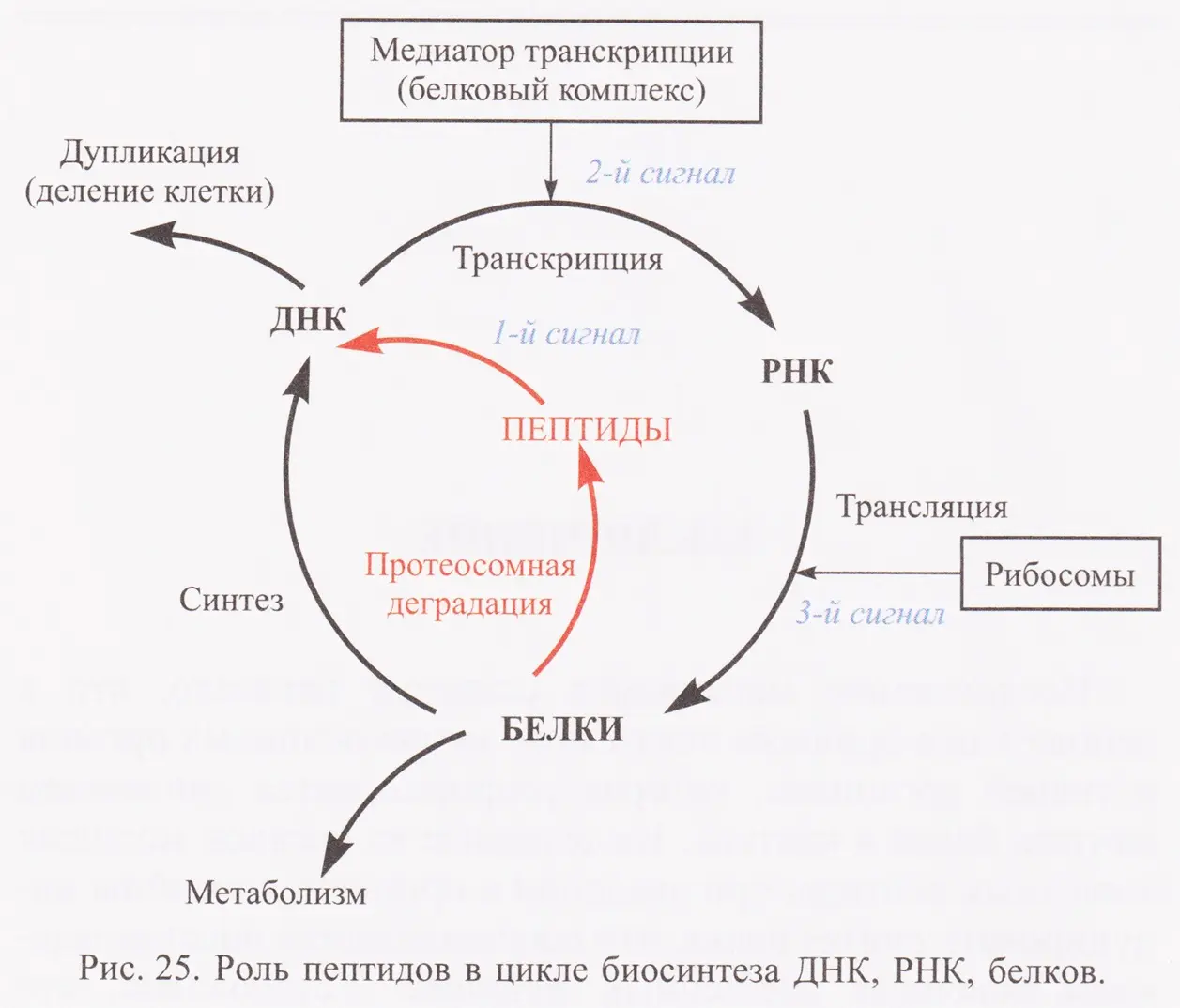
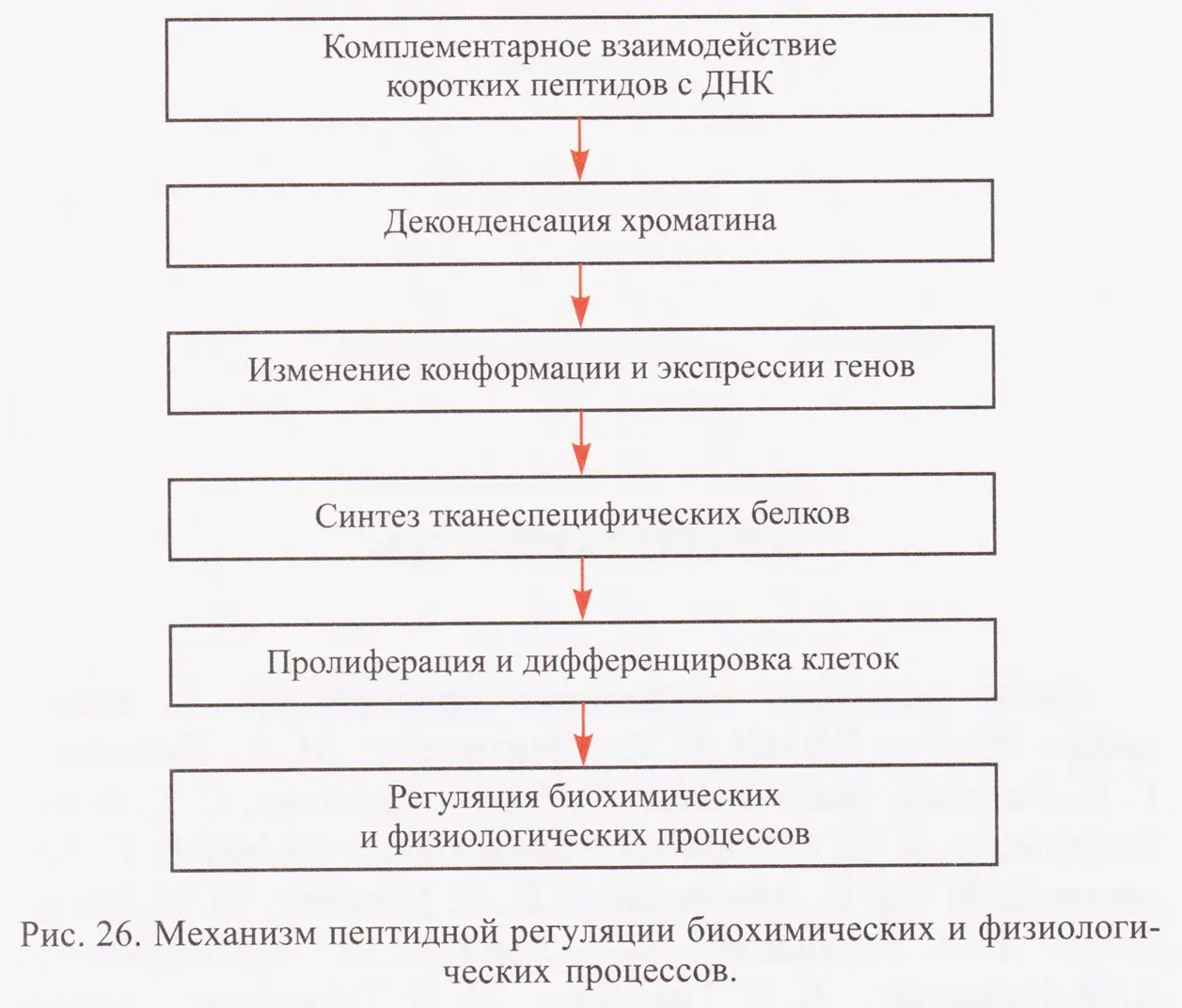
Заключение Исследования показали, что старение — это системный процесс, затрагивающий все уровни организма. Современные разработки в области пептидной регуляции открывают новые перспективы в борьбе со старением и возрастными заболеваниями. Клинические испытания подтвердили эффективность пептидной терапии для коррекции возрастных изменений (рис. 25, 26).
Дальнейшие исследования механизмов действия пептидов показали эффективность в применении к домашним животным и растениям. | |||||||||||||||||
| Просмотров: 580 | | |||||||||||||||||
| Всего комментариев: 0 | |
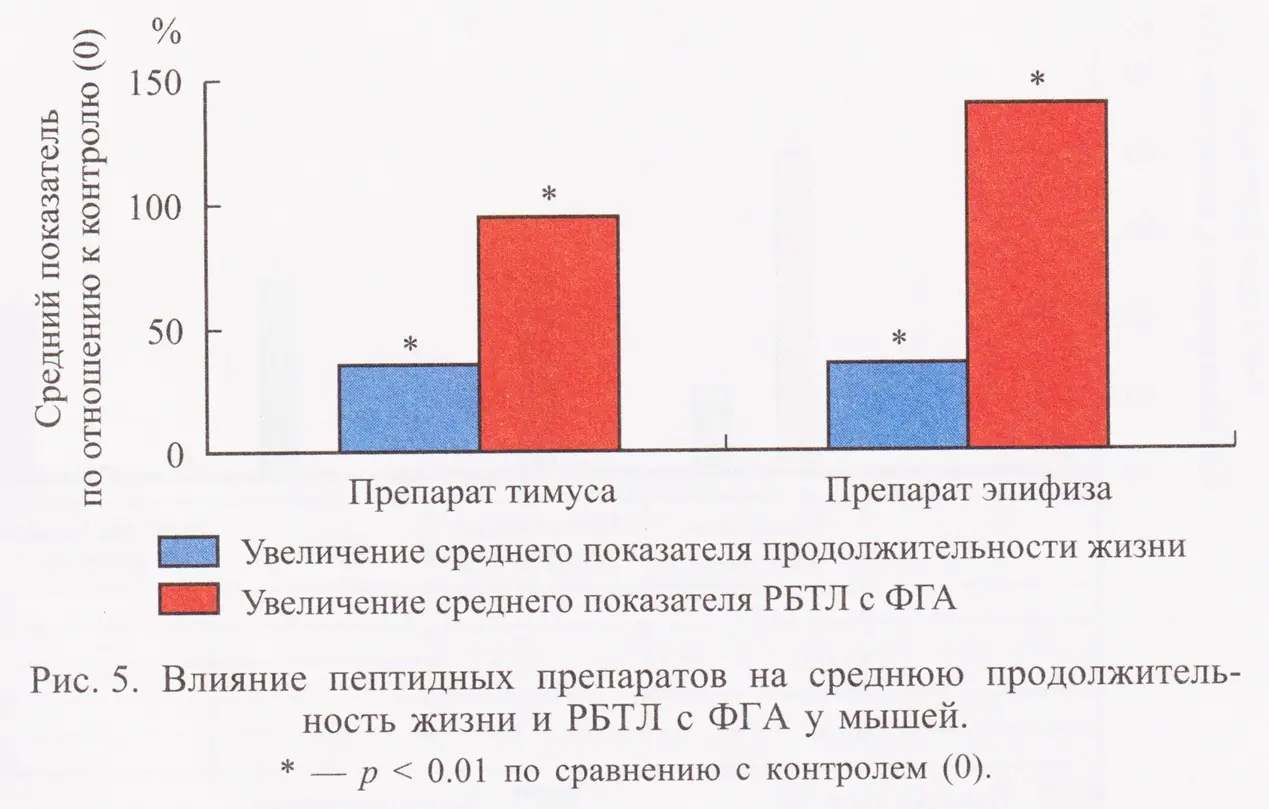 Для восстановления функций жизненно важных органов был создан специальный метод выделения низкомолекулярных пептидов из их экстрактов. Первым при старении страдает иммунитет. Экстракты тимуса и содержащиеся в них короткие пептиды были первыми веществами, использованными для коррекции возрастных иммунодефицитов. Эксперименты на макаках резусах показали впечатляющие результаты: препараты на основе пептидов эпифиза и тимуса — эпиталамин и тималин — продемонстрировали повышение средней продолжительности жизни лабораторных животных на 25–30 %. Наиболее значимый эффект увеличения максимальной продолжительности жизни был отмечен у мышей СВА при введении им пептида Ala-Glu-Asp-Gly и составил 42.3 % (рис. 5).
Для восстановления функций жизненно важных органов был создан специальный метод выделения низкомолекулярных пептидов из их экстрактов. Первым при старении страдает иммунитет. Экстракты тимуса и содержащиеся в них короткие пептиды были первыми веществами, использованными для коррекции возрастных иммунодефицитов. Эксперименты на макаках резусах показали впечатляющие результаты: препараты на основе пептидов эпифиза и тимуса — эпиталамин и тималин — продемонстрировали повышение средней продолжительности жизни лабораторных животных на 25–30 %. Наиболее значимый эффект увеличения максимальной продолжительности жизни был отмечен у мышей СВА при введении им пептида Ala-Glu-Asp-Gly и составил 42.3 % (рис. 5).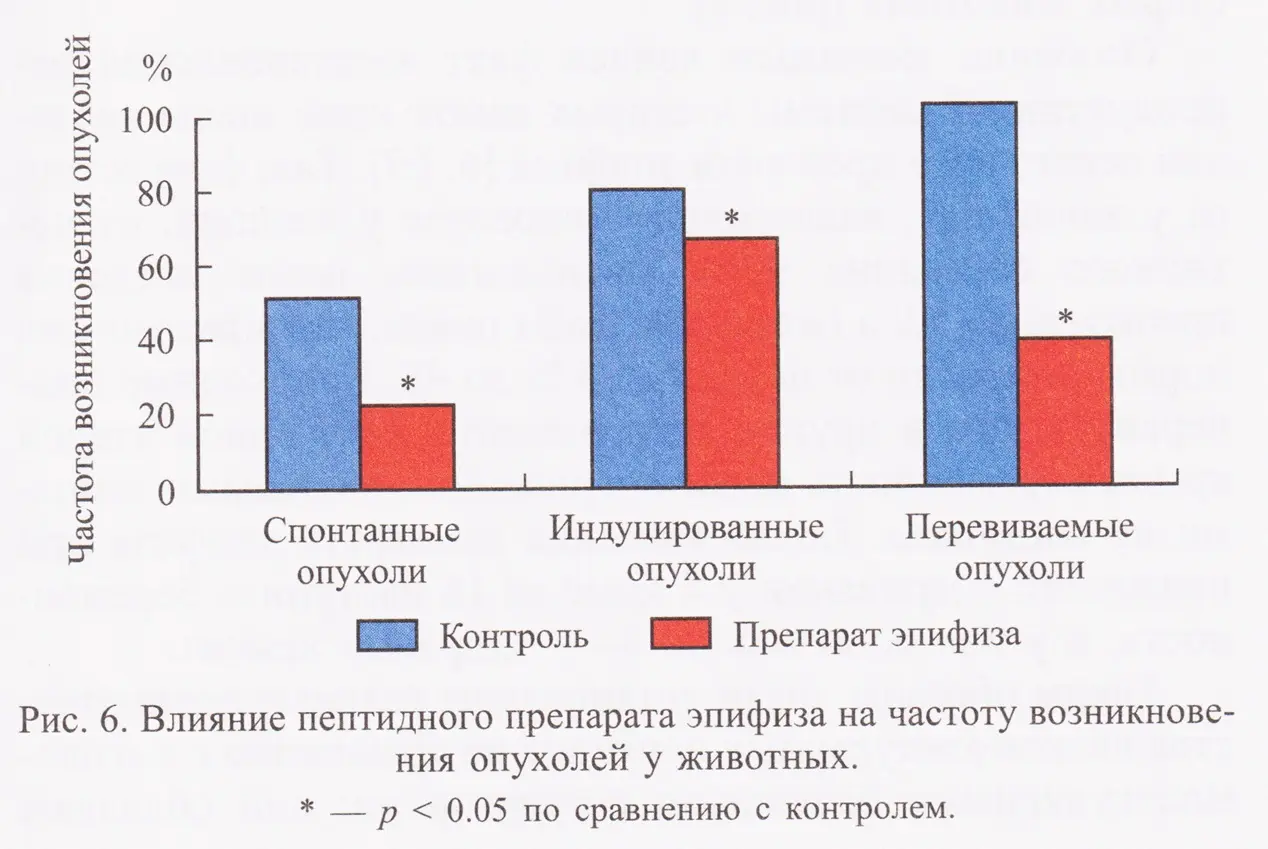 Короткие пептиды действуют выборочно: они активируют синтез белка именно в тех тканях, из которых были выделены. Было доказано, что даже у старых животных возможно восстановление репродуктивной функции и регенерация органов – у самок крыс после применения пептидов эпифиза восстанавливался нормальный гормональный цикл, и наступала беременность. Ключевым стало обнаружение противоопухолевой активности пептидов. При введении препаратов частота возникновения как спонтанных, так и индуцированных опухолей снижалась в 1,4–7 раз (рис. 6).
Короткие пептиды действуют выборочно: они активируют синтез белка именно в тех тканях, из которых были выделены. Было доказано, что даже у старых животных возможно восстановление репродуктивной функции и регенерация органов – у самок крыс после применения пептидов эпифиза восстанавливался нормальный гормональный цикл, и наступала беременность. Ключевым стало обнаружение противоопухолевой активности пептидов. При введении препаратов частота возникновения как спонтанных, так и индуцированных опухолей снижалась в 1,4–7 раз (рис. 6). Пептиды, такие как Lys-Glu, Ala-Glu-Asp-Gly, регулировали экспрессию сотен генов в сердце, мозге, печени, иммунной системе. Это доказывает их роль как универсальных молекул управления. Результат воздействия пептидов на генетическом уровне выражается в использовании биологического клеточного резерва различных органов и тканей организма, что составляет основу увеличения продолжительности жизни до видового предела (рис. 1).
Пептиды, такие как Lys-Glu, Ala-Glu-Asp-Gly, регулировали экспрессию сотен генов в сердце, мозге, печени, иммунной системе. Это доказывает их роль как универсальных молекул управления. Результат воздействия пептидов на генетическом уровне выражается в использовании биологического клеточного резерва различных органов и тканей организма, что составляет основу увеличения продолжительности жизни до видового предела (рис. 1).